Gases
Se denomina gas (palabra inventada por el científico flamenco Jan Baptista van Helmont en el siglo XVII, sobre el latín chaos) al estado de agregación de la materia en el cual, bajo ciertas condiciones de temperatura y presión, sus moléculas intereaccionan solo débilmente entre sí, sin formar enlaces moleculares, adoptando la forma y el volumen del recipiente que las contiene y tendiendo a separarse, esto es, expandirse, todo lo posible por su alta energía cinética. Los gases son fluidos altamente compresibles, que experimentan grandes cambios de densidad con la presión y la temperatura. Las moléculas que constituyen un gas casi no son atraídas unas por otras, por lo que se mueven en el vacío a gran velocidad y muy separadas unas de otras, explicando así las propiedades:
- Las moléculas de un gas se encuentran prácticamente libres, de modo que son capaces de distribuirse por todo el espacio en el cual son contenidos. Las fuerzas gravitatorias y de atracción entre las moléculas son despreciables, en comparación con la velocidad a que se mueven sus moléculas.
- Los gases ocupan completamente el volumen del recipiente que los contiene.
- Los gases no tienen forma definida, adoptando la de los recipientes que las contiene.
- Pueden comprimirse fácilmente, debido a que existen enormes espacios vacíos entre unas moléculas y otras.
A temperatura y presión ambientales los gases pueden ser elementos como el hidrógeno, el oxígeno, el nitrógeno, el cloro, el flúor y los gases nobles, compuestos como el dióxido de carbono o el propano, o mezclas como el aire.
Los vapores y el plasma comparten propiedades con los gases y pueden formar mezclas homogéneas, por ejemplo vapor de agua y aire, en conjunto son conocidos como cuerpos gaseosos, estado gaseoso o fase gaseosa.
Proceso Isotérmico
Se denomina proceso isotérmico o proceso isotermo al cambio reversible en un sistema termodinámico, siendo dicho cambio a temperatura constante en todo el sistema. La compresión o expansión de un gas ideal puede llevarse a cabo colocando el gas en contacto térmico con otro sistema de Capacidad calorífica muy grande y a la misma temperatura que el gas; este otro sistema se conoce como foco calórico. De esta manera, el calor se transfiere muy lentamente, permitiendo que el gas se expanda realizando trabajo. Como la energía interna de un gas ideal sólo depende de la temperatura y ésta permanece constante en la expansión isoterma, el calor tomado del foco es igual al trabajo realizado por el gas: Q = W.
Una curva isoterma es una línea que sobre un diagrama representa los valores sucesivos de las diversas variables de un sistema en un proceso isotermo. Las isotermas de un gas ideal en un diagrama P-V, llamado diagrama de Clapeyron, son hipérbolas equiláteras, cuya ecuación es P•V = constante.

Proceso Isobárico
El proceso isobárico es un proceso que al igual que el anterior, es termodinámico, pero en este caso, es la presión la variable que permanece constante.
En este tipo de procesos, el calor que se transfiere al sistema, con una presión constante, se relaciona con las demás variables a través de la siguiente ecuación:
En este tipo de procesos, el calor que se transfiere al sistema, con una presión constante, se relaciona con las demás variables a través de la siguiente ecuación:
ΔQ = ΔU + PΔV,
De donde:
Q, es el calor transferido al sistema
U, es la energía interna
P, es la presión (constante en este proceso)
V, es el volumen.
U, es la energía interna
P, es la presión (constante en este proceso)
V, es el volumen.
En una gráfica donde representemos presión, frente a volumen (P-V), resultará una línea horizontal.
En cambio, en la siguiente gráfica se representa V frente a T, donde se pueden apreciar diferentes líneas rectas; cada una de ellas refleja a una isobara, donde varían los valores de volumen y temperatura de una a otra.
En cambio, en la siguiente gráfica se representa V frente a T, donde se pueden apreciar diferentes líneas rectas; cada una de ellas refleja a una isobara, donde varían los valores de volumen y temperatura de una a otra.
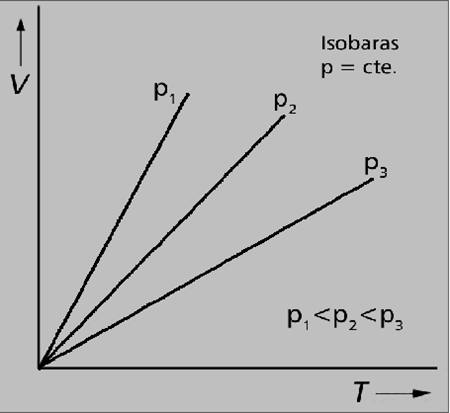
Las líneas isobáricas se utilizan también en la meteorología, para delimitar zonas donde hay diferencia de presión atmosférica o para unir zonas de igual presión.
No hay comentarios:
Publicar un comentario